〜大野会長による寄稿〜 続βグルカンの魅力 3.マイタケ(2)
〜大野会長による寄稿〜 続βグルカンの魅力 3
マイタケ(2)
宿前研究室では、1982年度からマイタケの抗腫瘍性多糖に関して本格的に研究を進めることとなった。多糖化学のチームと腫瘍免疫のチームが双方向から研究を同時にスタートした。1980年代初頭は、分子生物学を研究利用できる状態に至っておらず、オーソドックスな多糖の分離、構造解析、構造活性相関、のアプローチをとることとなった。構造と活性の関連性を追求する折に、常に悩まされるのが、比活性である。酵素タンパク質の精製過程で比活性の上昇を求めるのと同じ考え方である。活性本体は多糖であると信じてはいたものの、その確証を得るためには、徐タンパクされ、単一性の確認された多糖が動物モデルで強い抗腫瘍活性を示すことの証明が必要であった。前稿で示した通り、熱水抽出物GFEに活性があることを見出していたので、これを起点とした。子実体は脂質を多量に含むので、脱脂・乾燥、オートクレーブ抽出、可溶部を透析、濃縮、エタノール沈殿にて多糖画分を集めた。これを徐タンパクするために銅複合体法を用いた。すなわち、多糖画分を1% NaOHに溶解、7%の硫酸銅溶液を添加して多糖を沈殿、10%酢酸で沈殿を可溶化、透析後にイオン交換樹脂で金属を除去し、凍結乾燥した。Sepharose CL-2Bカラムで多糖部分は単一ピークとなり、低分子領域に若干のUV吸収を示し、タンパク質含量は4%程度に減少した。GFEのタンパク質含量(約30%)と比較し、かなり低下したので、この画分をGF-1と命名し活性評価した。ICRマウスに移植したSarcoma 180固形腫瘍への効果を検討したところ、腫瘍移植1−10日間連投後、5週間目の平均腫瘍重量は、コントロール群で約5グラムに対し、0.5、1、2、3、4、5ミリグラム投与群において、抑制率は概ね、83, 92, 99, 93, 99, 99%となり、腫瘍が完全退縮した個体もおり、0.5 – 5ミリグラムの濃度範囲のいずれも有効であった。投与経路は腹腔内、静脈内、腫瘍内は有効であったが、経口投与は無効であった。さらに、同種同系の抗腫瘍モデルを用いたところ、Meth A, MM46に対して有効であったが、MH134, EL-4には無効であった。
(以上は、Suzuki et al., J. Pharm. Dyn., 7, 492, 1984)。
前述の方法は、各ステップでの比活性の上昇を重視する方法であるが、抗腫瘍効果の評価は2か月を要する。多糖化学のチームはマイタケ多糖の分画を先行し、ある程度の画分が集まったところで活性を一括して評価することとした。抽出物の調製にあたり、効率化を目指し子実体を細切したもの(CF)と粉末化したもの(PF)を作成し、それらから抽出し比較検討した。抽出法の確立のため種々の試行錯誤を行い、オートクレーブで熱水抽出の後、10% NaOH溶液を用いて、低温(4℃)ならびに高温(65℃)で抽出することとした。NaOH抽出物は中和・透析後に可溶部と不溶部に分離した。一連の画分を得たのち、メチル化、NMR、ゲルろ過、アミラーゼ分解などの分析を行うとともに、抗腫瘍活性を測定した。強い活性はNaOH抽出可溶部に認められ、構造解析の結果、6分岐β-1,3-グルカンを主成分とすることが分かった。熱水抽出画分は多量のαグルカンを含有し、アミラーゼで分解されたが、活性は残存したので、本体はNaOH抽出物と同様の構造であると推定された。
(以上は、Ohno et al., Chem. Pharm. Bull., 32, 1142, 1984)。
上記で課題として残されたのは、熱水抽出画分、すなわち起点として用いたGFEの活性本体は精製できないのか、という点である。アルカリ抽出物の比活性から考察すると熱水抽出中の活性本体の含量は極微量であり、その割合を推定することすら困難に思われた。現時点であれば、特異抗体や特異的な結合蛋白質でのアフィニティー精製も可能と思われるが、当時はそれらの技術は開発以前であった。この問題を解決するために、我々がとったアプローチは、あらかじめアミラーゼ処理した子実体から熱水抽出物を作成するというものである。当時、13C-NMRの技術が著しく進歩し、1cm径の測定チューブにキノコの重水懸濁液を注入し、直接NMR測定することが可能であった。径が太いことから、感度も稼げるので、キノコの中で水和している分子のNMR信号を抽出前であっても測定可能であった。アミラーゼ処理前後のNMRチャートを比較したところ、αグルカンが除去されたことがわかった(下図)。この処理菌体を熱水抽出し、イオン交換クロマトにて中性画分を集め、活性測定並びにメチル化分析等を行った。この多糖をgrifolan 1Nと命名した。grifolan 1Nは、6分岐β-1,3-構造をとり、0.02ミリグラムx5回投与で強い抗腫瘍活性を示した。これらの解析で、マイタケ熱水抽出物の活性本体を解明することができた。
(以上は、Ohno et al., Chem. Pharm. Bull., 33, 4522, 1985)。
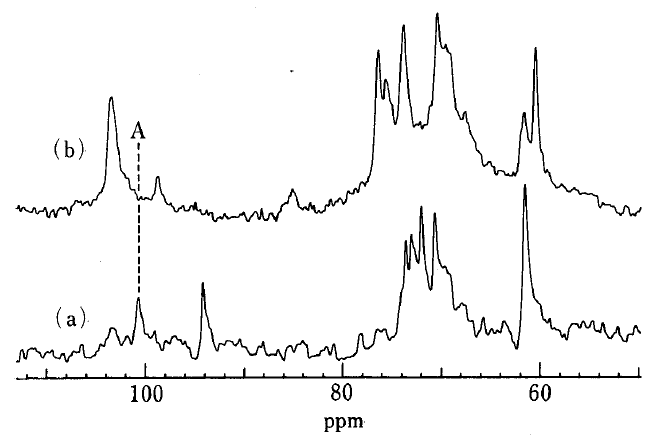
アミラーゼ処理したマイタケ子実体粉末を重水に懸濁し、13C-NMRを測定。
(a)は処理前、(b)は処理後。Aはαグルカンのアノメリック炭素シグナル。
β‐グルカン協議会会長
東京薬科大学 薬学部教授
大野 尚仁